金が金色なのはなぜ?
みなさんこんにちは!パスカルです!!
先々週はすっかりブログの更新を忘れていました…
実験レポートに追われてましたね、はい。
Twitterでも毎週実験の情報をお届けしていますが、やはり週2日実験というのはなかなかですね😅
でも理学部って感じがしてとっても充実しています!!!
さてさて、今回は題名にもあります通り金が金色なのはなぜ?について考えていきます!
なぜこれについて書いていくかというと、2年生で「有機元素化学」という講義がありまして、先週に相対論効果について触れました。相対論効果についてよく知っていくと、金が金色である理由が分かるということを先生が仰っていましたので、気になって調べてみたわけです!
ちょっと難しいかもしれませんが、できるだけ分かりやすく説明しますので、頑張っていきましょう!!!

電子軌道
金のお話に行く前に、2つ知ってもらわなければならないことがあるためそこから説明します!
1つ目は電子軌道です!
高校では、「電子が原子核の周りを回っており、K・L・M・N殻といった電子殻に規則正しく配置される」と習ったのではないでしょうか?
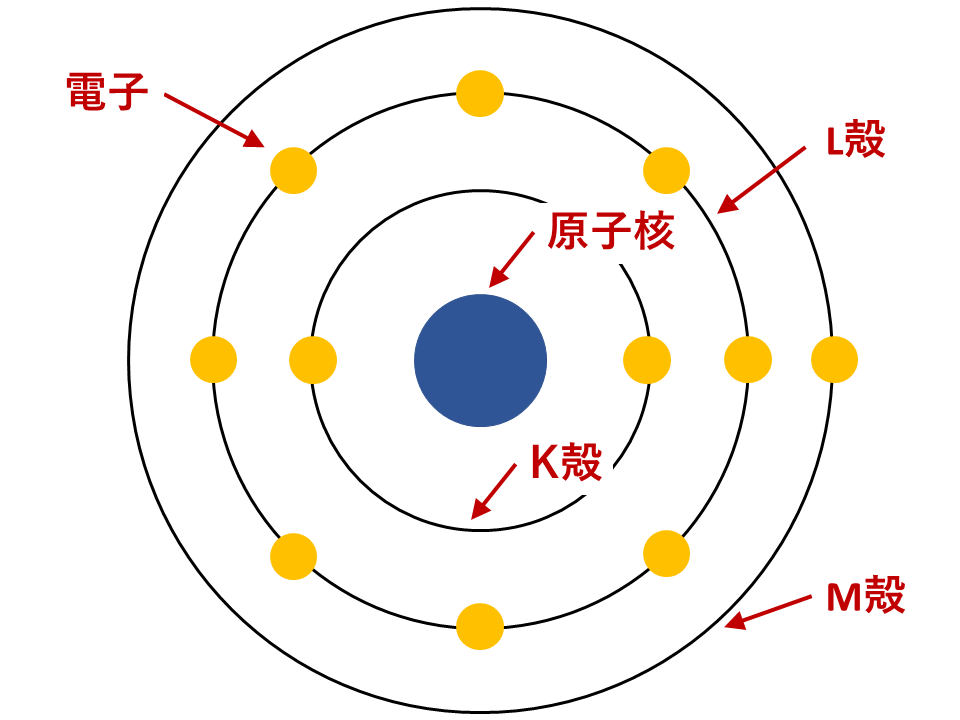
https://brain.vicolla.jp/2018/09/06/electron-configuration/
しかし!電子が原子核の周りを回っているというのは間違いです。
回っているのではなく、電子は原子核の周りにもやもやと存在しているんです。
そのため、電子がどこに存在しているかは特定することができません。
そこで、電子が存在している可能性が高い場所として「軌道」という概念が生まれました。
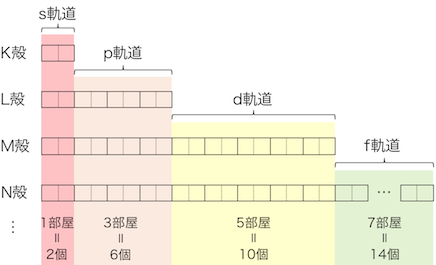
http://www.jukenmemo.com/chemistry/theory/electron-configuration/
今まで習ったK・L・M・N殻などが細かく分けられたと考えてもらって構いません。ここで重要なのは、1つの軌道には2つの電子しか入らないということです!
え、p軌道やd軌道はどうなってるの?と思うかもしれませんが、これはx、y、zの方向性がそれぞれ存在するため、p軌道は合計で6個の電子を入れることができます。


上がs軌道、下がp軌道です。
p軌道だと単純ですが、d軌道になると少し複雑になってきますね…。
ちなみに、K殻の電子は1s軌道、L格の電子は2s軌道と2p軌道…という感じになります。
高校生の方は聞いたことがあるかもしれませんが、電子は軌道に順番に入っていくわけではありません。「遷移元素は違うよー」と聞いたことありませんか?
これについては話すと長くなってしまうため、またの機会にお話ししようと思います!!
軌道というものを理解するのに結構時間がかかると思いますが、これを理解するだけでたくさんのことが見えてきます!!
よく分からない!って人は、電子が入る場所が決まっているんだよくらいに思っておいてください。
相対性理論とは
2つ目は相対論効果です!
相対論効果には名前の通り、アインシュタインの相対性理論が関係しています!
原子は、正の電荷を持つ陽子と電荷を持たない中性子から成る原子核と、その周りにある負の電荷を持った電子から成り立っていますよね。
ということは、大きな(原子番号が大きい)原子になると正の電荷の影響がとても大きくなることが想像できます。
そのとき電子は、ものすごい速さで原子核の周りを回っているんです。
(+が強くなるなら電子は原子核にくっつくじゃん!って思ったあなた!そんなことがあり得てしまったら、核反応がそこら中で起きていることになってしまいますよ!)
相対性理論では、「光は万物の中で最速であり、何も超えることはできない」とされていますよね。
つまり、とても大きな原子においては電子の速度は光速に近づきます!
光速に近づくと、静止状態より電子の質量が増え、それにより電子がより核に引き付けられて、s軌道が収縮して安定化します。
これが相対論効果です。
s軌道が近づくと、外側にあるd軌道やf軌道は電荷のバランスをとるために逆に外に張り出すことになるため、d軌道とf軌道のエネルギーが上がることになります!
エネルギーが上がると言うことは、d軌道が不安定になるということです!
ちなみに、金は原子番号79の元素ですが、金の1s軌道の電子の速度は光速の58%ほどになります。
となると、相対論効果を無視できなくなるんです。
上記の説明は、直観的に理解してもらうために式を省いて日本語だけで説明していますが、式を見た方が分かりやすいかもしれません。式に関しては以下のサイトを見てみてください!!↓
金が金色である理由
ということで、ここまで分かるとようやく金が金色である理由が分かります!!
金の電子配置は以下の通りです。
Au:(1s)²(2s)²(2p)⁶(3s)²(3p)⁶(3d)¹⁰(4s)²(4p)⁶(4d)¹⁰(4f)¹⁴(5s)²(5p)⁶(5d)¹⁰(6s)¹
ということで、最もエネルギーが高い軌道が6s軌道であり、その次に高い軌道が5d軌道となります。
ではエネルギーはどうなるのか。

https://www.toho-u.ac.jp/sci/chem/column/gold_color/032128.html
Rは相対論効果を考慮した時のエネルギー、NRは考慮しないときのエネルギーを示しています。
これを見ると分かるように、相対論効果を考えると、6s軌道は収縮しており安定化してエネルギーが低くなっているため、5d軌道の電子が6s軌道に移動するために必要なエネルギーが銀に比べて小さくなっていますよね!!
この移動に必要な最低限のエネルギーがおよそ2.4eVであり、光の波長にすると520nmとなります。これは可視光領域に当たります。
これよりも短い波長の光(エネルギーの高い光)を5dから6s軌道への移動に使うために吸収します。金では紫から青色の光を吸収し、そしてそれよりも長い波長の光である黄色や赤色の光を反射します。
だから金色なんです!!!
ちなみに銀では、4d軌道から5s軌道への移動に必要なエネルギーは金より大きく3.7eVであり、光の波長にすると335nmとなるため、可視光領域の光を吸収しません。そのため、白く見えるんですね。
まとめ
さて今回は、金が金色である理由を見てきました!
知識がない人には結構理解するのが大変かもしれません。(説明が下手くそですみません…)
私はこれを調べたときに結構感動しました🌟
金だから金色なのではなく、そこにはちゃんと理由があったんですね。
当たり前のことでも理由を探してみると面白いかもしれません😊
今日はここまで!!!
参考サイト
東北大学「金の色と相対論効果」(最終閲覧日2020年7月13日)
https://www.toho-u.ac.jp/sci/chem/column/gold_color/032128.html
